| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
1.7. Отличительные свойства газов
Основная особенность газа, с которой связано большинство его характерных свойств, заключается в том, что молекулы газа находятся на большом удалении друг от друга и каждая молекула с динамической точки зрения изолирована от других молекул в течение большей части своей жизни. При температуре  и давлении в одну атмосферу число молекул в одном кубическом сантиметре газа равно
и давлении в одну атмосферу число молекул в одном кубическом сантиметре газа равно  (оно называется числом Лошмидта, а тот факт, что оно одинаково для всех газов, известен как закон Авогадро), поэтому, если бы молекулы были размещены в углах кубической решетки, расстояние между соседними молекулами было бы
(оно называется числом Лошмидта, а тот факт, что оно одинаково для всех газов, известен как закон Авогадро), поэтому, если бы молекулы были размещены в углах кубической решетки, расстояние между соседними молекулами было бы  см. Диаметр молекулы точно не
см. Диаметр молекулы точно не
определен, однако его обоснованной мерой служит расстояние между центрами двух отдельных молекул, на котором межмолекулярная сила изменяет знак (см. § 1.1). Для многих простых молекул этот эффективный диаметр  находится в интервале
находится в интервале  так что средняя величина удаления молекул друг от друга в указанном выше смысле составляет величину порядка
так что средняя величина удаления молекул друг от друга в указанном выше смысле составляет величину порядка  На этом расстоянии силы сцепления молекул, действующие между ними, столь малы, что большую часть своей жизни молекулы движутся свободно по прямым линиям с постоянной скоростью (мы предполагаем, что они электрически нейтральны). Понятие столкновения между двумя молекулами также точно не определено, однако если определить столкновение как событие, происходящее всякий раз, когда одна молекула приближается к другой настолько близко, что действующая между ними сила становится отталкивающей, то можно вычислить среднее расстояние, проходимое молекулой между столкновениями и равное
На этом расстоянии силы сцепления молекул, действующие между ними, столь малы, что большую часть своей жизни молекулы движутся свободно по прямым линиям с постоянной скоростью (мы предполагаем, что они электрически нейтральны). Понятие столкновения между двумя молекулами также точно не определено, однако если определить столкновение как событие, происходящее всякий раз, когда одна молекула приближается к другой настолько близко, что действующая между ними сила становится отталкивающей, то можно вычислить среднее расстояние, проходимое молекулой между столкновениями и равное  или
или  с учетом приведенной выше оценки для
с учетом приведенной выше оценки для 
Представление о газе как о скоплении молекул, движущихся почти свободно, исключая случайные столкновения, лежит в основе кинетической теории газов. В этой теории принято рассматривать свойства совершенного газа, молекулы которого не оказывают никакого силового воздействия друг на друга, не считая актов столкновений, и занимают пренебрежимо малый объем. (Частота столкновений молекулы стремится к нулю вместе с объемом молекул, однако она играет малую роль в теории и достаточно лишь знать, что некоторые столкновения происходят.) Из приведенных выше числовых данных кажется вероятным, что при нормальных условиях реальные газы обладают свойствами, которые мало отличаются от свойств гипотетического совершенного газа, и наблюдения показывают, что это именно так; в действительности некоторые из эмпирических законов, открытые ранее при исследовании свойств газов, такие, как закон Бойля или закон Шарля, можно вывести как свойства совершенного газа. Поэтому описание элементарных свойств газов целесообразно начать с изучения их отклонений от свойств совершенного газа.
Мы, естественно, в полной мере используем мощные идеи и результаты классической термодинамики (§ 1.5) и менее строгие результаты теории переноса (§ 1.6). Выводы двух предыдущих параграфов не зависят от молекулярной структуры вещества, и плата за такую общность отчасти состоит в том, что в них было получено мало подробных и конкретных результатов. Если теперь несколько снизить общность рассуждений и перейти к конкретным средам со сравнительно простой молекулярной структурой, таким, как, например, совершенный газ, то появится возможность получить значительно больше дополнительных результатов.
Совершенный газ в равновесном состоянии
Рассмотрим сначала покоящийся совершенный газ в состоянии термодинамического равновесия в смысле, указанном § 1.5: все параметры газа не зависят от координат и времени, так что процессов переноса нет. Предположим прежде всего, что все молекулы одинаковы и каждая имеет массу  где
где  числовая плотность молекул. Хотя молекулы подчиняются динамическим законам, их так много, что можно дать соответствующее статистическое описание движения. Поэтому введем плотность распределения вероятностей; эту плотность для скорости молекул и обозначим
числовая плотность молекул. Хотя молекулы подчиняются динамическим законам, их так много, что можно дать соответствующее статистическое описание движения. Поэтому введем плотность распределения вероятностей; эту плотность для скорости молекул и обозначим  Произведение
Произведение  есть вероятность того, что скорость данной молекулы в любой момент времени имеет компоненты, значения которых лежат в интервалах и
есть вероятность того, что скорость данной молекулы в любой момент времени имеет компоненты, значения которых лежат в интервалах и  с другой стороны, произведение
с другой стороны, произведение  можно рассматривать как относительное количество молекул в данном объеме, которые в каждый момент времени имеют компоненты скорости в указанных пределах. Функция
можно рассматривать как относительное количество молекул в данном объеме, которые в каждый момент времени имеют компоненты скорости в указанных пределах. Функция  тождественно удовлетворяет условию
тождественно удовлетворяет условию

Предположим, что столкновения молекул нарушают какое-либо заданное начальное распределение скоростей, так что в состоянии равновесия функция  зависит только от модуля скорости
зависит только от модуля скорости  и не зависит от вида молекул.
и не зависит от вида молекул.
Простое соотношение между давлением и средними параметрами молекулы служит хорошим примером того, что можно достичь в статистической модели совершенного газа. Для получения этого соотношения рассмотрим перенос количества движения молекул газа, движущихся в обоих направлениях через неподвижный элемент поверхности  с нормалью
с нормалью  Количество молекул, пересекающих в единицу времени элемент поверхности со скоростями, компоненты которых отличаются не более чем на
Количество молекул, пересекающих в единицу времени элемент поверхности со скоростями, компоненты которых отличаются не более чем на  от скорости и (переход молекул отсчитывается в ту сторону, на которой направление нормали
от скорости и (переход молекул отсчитывается в ту сторону, на которой направление нормали  положительное), равно
положительное), равно  каждая из этих молекул переносит через элемент поверхности количество движения
каждая из этих молекул переносит через элемент поверхности количество движения  Следовательно, полный поток количества движения через этот элемент в результате движения молекул равен
Следовательно, полный поток количества движения через этот элемент в результате движения молекул равен

Благодаря симметрии распределения скоростей компонента этого потока количества движения в направлении касательной к
элементу поверхности равна нулю и нужно рассматривать только компоненту по нормали к ней. Кроме того, сила, действующая непосредственно между молекулами по любую сторону от элемента поверхности, равна нулю для совершенного газа, поэтому напряжение в газе порождается только потоком количества движения. Из этого следует, что напряжение в совершенном газе представляет собой нормальное давление

где черточка означает среднее по всем молекулам в единице объема. Среднее значение в (1.7.1) не зависит от направления нормали  так что можно написать
так что можно написать

Если в газе имеется несколько различных видов молекул, то подобное рассуждение справедливо для каждого из них отдельно; поэтому, применяя очевидные обозначения, получаем

Это рассуждение не дает давления газа на твердую границу, однако выражение (1.7.3) справедливо и на твердой границе, поскольку условия механического равновесия газа требуют, чтобы давление  было непрерывным всюду внутри газа (см. (1.4.2)) и постоянным при отсутствии массовых сил.
было непрерывным всюду внутри газа (см. (1.4.2)) и постоянным при отсутствии массовых сил.
Функция распределения скоростей  для каждой составной части газа является одной из фундаментальных в кинетической теории, и было предпринято много попыток найти ее вид для совершенного газа в состоянии равновесия. Ни один из имеющихся выводов полностью не свободен от различных предположений, хотя все они дают один и тот же результат, который также находится в удовлетворительном соответствии с наблюдением, и почти нет сомнений в его справедливости. Вероятно, наиболее удовлетворителен вывод с использованием методов статистической механики. Такой «метод наиболее вероятного состояния» дает полезную дополнительную информацию, и здесь будут изложены общие рёзультаты, полученные по этому методу
для каждой составной части газа является одной из фундаментальных в кинетической теории, и было предпринято много попыток найти ее вид для совершенного газа в состоянии равновесия. Ни один из имеющихся выводов полностью не свободен от различных предположений, хотя все они дают один и тот же результат, который также находится в удовлетворительном соответствии с наблюдением, и почти нет сомнений в его справедливости. Вероятно, наиболее удовлетворителен вывод с использованием методов статистической механики. Такой «метод наиболее вероятного состояния» дает полезную дополнительную информацию, и здесь будут изложены общие рёзультаты, полученные по этому методу 
Указанные результаты касаются распределения вероятностей для всех параметров, необходимых для определения состояния молекулы, включая три компоненты количества движения
молекулы как целого. Если предположить, что вращательные и колебательные формы движения молекулы описываются классическими законами (в действительности при некоторых условиях необходимо привлекать квантовую теорию, о чем речь пойдет ниже), то в целом состояние молекулы с  степенями свободы в каждый момент времени может быть представлено с помощью
степенями свободы в каждый момент времени может быть представлено с помощью  обобщенных координат
обобщенных координат  соответствующих им
соответствующих им  обобщенных импульсов
обобщенных импульсов  координаты
координаты  можно считать декартовыми координатами центра масс молекулы и тогда
можно считать декартовыми координатами центра масс молекулы и тогда  а другие
а другие  степени свободы относятся к вращательным и колебательным формам движения. В совершенном газе молекулы динамически не зависят друг от друга, так что в соответствии с данными значениями обобщенных координат и моментов существует полная энергия молекулы
степени свободы относятся к вращательным и колебательным формам движения. В совершенном газе молекулы динамически не зависят друг от друга, так что в соответствии с данными значениями обобщенных координат и моментов существует полная энергия молекулы  включающая как часть энергию их поступательного движения. Следовательно, вероятность того, что для данной молекулы в любой момент времени значения ее обобщенных координат и импульсов лежат внутри интервалов от до
включающая как часть энергию их поступательного движения. Следовательно, вероятность того, что для данной молекулы в любой момент времени значения ее обобщенных координат и импульсов лежат внутри интервалов от до  от
от  до
до  равна
равна

где постоянные С и а не зависят от  Постоянную С можно определить из тождества
Постоянную С можно определить из тождества

если знать зависимость энергии  от обобщенных координат
от обобщенных координат  причем интеграл в (1.7.5) берется по всевозможным значениям
причем интеграл в (1.7.5) берется по всевозможным значениям  постоянная С поэтому зависит только от вида молекул и от параметра распределения а. Выражение (1.7.4) широко используется и известно как классическое (т. е. неквантовое) распределение Болъцмана.
постоянная С поэтому зависит только от вида молекул и от параметра распределения а. Выражение (1.7.4) широко используется и известно как классическое (т. е. неквантовое) распределение Болъцмана.
Если на газ не действуют массовые силы, то энергия  а следовательно, также и выражение (1.7.4) не зависят от координат
а следовательно, также и выражение (1.7.4) не зависят от координат  поэтому плотность газа постоянна, как это и предполагалось ранее.
поэтому плотность газа постоянна, как это и предполагалось ранее.
Независимо от внутренней структуры молекулы можно написать, что энергия

и допустимые значения  лежат в интервале от
лежат в интервале от  до
до  Интегрирование в (1.7.5) по
Интегрирование в (1.7.5) по  можно провести
можно провести
отдельно, что дает соотношение

для определения константы С. Тогда вероятность нахождения молекулы в данном состоянии с компонентами скорости, отличающимися не более чем на  от компонент скорости и, после деления на
от компонент скорости и, после деления на  равна
равна

это хорошо известное максвелловское распределение скоростей молекул  полученное впервые Максвеллом на основе предположения о статистической независимости трех компонент скорости (которое, очевидно, корректно, но строго доказать его трудно). Единственный параметр а, который необходим для полного вычисления распределения скоростей молекул, связан со средней энергией их поступательного движения, следовательно,
полученное впервые Максвеллом на основе предположения о статистической независимости трех компонент скорости (которое, очевидно, корректно, но строго доказать его трудно). Единственный параметр а, который необходим для полного вычисления распределения скоростей молекул, связан со средней энергией их поступательного движения, следовательно,

Если газ представляет собой смесь молекул различного вида, то распределение (1.7.4) Больцмана и распределение (1.7.8) Максвелла применимы к каждому виду молекул отдельно. Кроме того, из рассуждения, приводящего к выражению (1.7.4), следует, что параметр а имеет одно и то же значение для всех молекул, из которых состоит газ; можно показать, что это необходимо. В самом деле, если в качестве  взять обобщенные координаты и импульсы пар молекул различного вида, то в этом случае параметр
взять обобщенные координаты и импульсы пар молекул различного вида, то в этом случае параметр  равен сумме энергий двух молекул в отдельности и имеется шесть поступательных степеней свободы. Таким образом, если
равен сумме энергий двух молекул в отдельности и имеется шесть поступательных степеней свободы. Таким образом, если  скорости двух молекул с массами
скорости двух молекул с массами  соответственно, то из (1.7.9) следует
соответственно, то из (1.7.9) следует

т. е. что все молекулы в смеси газов имеют одинаковую среднюю энергию поступательного движения. Ранее было показано, что молекулы создают давление газа в соответствии с энергией их поступательного движения; теперь выражение (1.7.3) можно
переписать в виде

где  числовая плотность молекул одного вида; выражение (1.7.11) показывает, что вклад в давление от каждой составной части смеси пропорционален числу молекул этой составной части в единице объема.
числовая плотность молекул одного вида; выражение (1.7.11) показывает, что вклад в давление от каждой составной части смеси пропорционален числу молекул этой составной части в единице объема.
Соотношение (1.7.10) является одним из проявлений принципа равномерного распределения энергии по степеням свободы. Этот принцип применим к любой из обобщенных координат и любому из импульсов молекулы, которые входят в выражение энергии молекул с в виде квадратичных слагаемых и область допустимых значений которых простирается от  до Так, предположим, что функция
до Так, предположим, что функция  в (1.7.6) имеет такой вид, что
в (1.7.6) имеет такой вид, что

где коэффициент а не зависит от обобщенной координаты  Тогда в соответствии с (1.7.4) и (1.7.5) среднее значение величины
Тогда в соответствии с (1.7.4) и (1.7.5) среднее значение величины  при фиксированных значениях всех других обобщенных координат и импульсов равно
при фиксированных значениях всех других обобщенных координат и импульсов равно

Это среднее значение не зависит от выбранных значений координат и импульсов, за исключением  и поэтому оно справедливо и в общем случае. Следовательно, средняя энергия, связанная с любой обобщенной координатой и любым импульсом, которые появляются в виде дополнительного квадратичного слагаемого, равна
и поэтому оно справедливо и в общем случае. Следовательно, средняя энергия, связанная с любой обобщенной координатой и любым импульсом, которые появляются в виде дополнительного квадратичного слагаемого, равна  Этот дополнительный квадратичный член может выражать кинетическую энергию поступательного движения в одном из трех взаимно перпендикулярных направлений, или кинетическую энергию вращения молекулы относительно одной из ее главных осей, или кинетическую энергию колебательной формы ее движения, или потенциальную энергию, связанную с малой деформацией молекулы относительно ее равновесной формы. Если классические законы динамики применимы к молекулам, то средняя полная энергия одноатомной молекулы с массой, сосредоточенной в точке, равна
Этот дополнительный квадратичный член может выражать кинетическую энергию поступательного движения в одном из трех взаимно перпендикулярных направлений, или кинетическую энергию вращения молекулы относительно одной из ее главных осей, или кинетическую энергию колебательной формы ее движения, или потенциальную энергию, связанную с малой деформацией молекулы относительно ее равновесной формы. Если классические законы динамики применимы к молекулам, то средняя полная энергия одноатомной молекулы с массой, сосредоточенной в точке, равна  энергия жесткой двухатомной молекулы с ненулевым моментом инерции относительно двух главных осей равна
энергия жесткой двухатомной молекулы с ненулевым моментом инерции относительно двух главных осей равна  энергия двухатомной
энергия двухатомной
молекулы, атомы которой могут колебаться вдоль соединяющей их прямой, равна 
В смеси газов распределение координат и импульсов молекул каждого вида определяется значением параметра а функции распределения (1.7.4), который имеет одно и то же значение для каждой компоненты смеси. Этот факт можно сформулировать в виде утверждения, что если два различных газа находятся в тепловом равновесии, то соответствующие значения параметра а обоих газов равны. Температура определяется как величина, которая обладает тем же самым свойством, и поэтому естественно найти связь между параметром а и температурой газа. Это можно сделать путем сравнения равенства (1.7.11) и термодинамического выражения для давления  В § 1.5 было показано, что для любой среды
В § 1.5 было показано, что для любой среды

и

Соотношение Максвелла (1.5.15) позволяет записать последнее равенство в виде

В совершенном газе по определению внутренняя энергия есть сумма отдельных видов энергии молекул на единицу массы и не зависит от расстояний между молекулами, т. е. не зависит от плотности  Следовательно, для совершенного газа
Следовательно, для совершенного газа

Известно, что при постоянной плотности давление  пропорционально температуре
пропорционально температуре  (закон Шарля), и, согласно равенству (1.7.11),
(закон Шарля), и, согласно равенству (1.7.11),

где k — постоянная, называемая постоянной Болъцмана. Если единица температуры определена так, что абсолютная температура  при температуре плавления льда (соответствующей 0° С), то
при температуре плавления льда (соответствующей 0° С), то

Равенство (1.7.11) для давления превращается в уравнение состояния совершенного газа

где  средняя масса молекулы газа, а параметр
средняя масса молекулы газа, а параметр  известен как газовая постоянная (для сухого воздуха
известен как газовая постоянная (для сухого воздуха  Одно из следствий уравнения состояния состоит в том, что коэффициент теплового расширения совершенного газа
Одно из следствий уравнения состояния состоит в том, что коэффициент теплового расширения совершенного газа

Для изотермического коэффициента сжимаемости имеем выражение

показывающее, что относительные изменения давления  и плотности
и плотности  при постоянной температуре
при постоянной температуре  равны; адиабатический же коэффициент сжимаемости, как уже известно, равен изотермическому, умноженному на
равны; адиабатический же коэффициент сжимаемости, как уже известно, равен изотермическому, умноженному на  (см. (1.5.6)).
(см. (1.5.6)).
Тот факт, что для совершенного газа  зависит только от температуры
зависит только от температуры  упрощает некоторые общие выражения для удельной теплоемкости. Две основные теплоемкости, определяемые равенствами (1.5.5), принимают вид
упрощает некоторые общие выражения для удельной теплоемкости. Две основные теплоемкости, определяемые равенствами (1.5.5), принимают вид

отсюда получаем закон Карно

который, как установлено, выполняется с погрешностью, не превышающей  для воздуха при нормальных температуре и давлении. Теплоемкости
для воздуха при нормальных температуре и давлении. Теплоемкости  подобно
подобно  зависят только от температуры, и функции состояния
зависят только от температуры, и функции состояния  можно записать так:
можно записать так:

Когда молекулы совершенного газа имеют простую структуру, можно еще упростить выражения для внутренней энергии и удельных теплоемкостей. Для одноатомных молекул в виде точечных масс, обладающих только энергией поступательного движения, средняя энергия равна  так что
так что

В более общем случае, если для каждой молекулы газа энергия  выражается в виде суммы
выражается в виде суммы  членов, каждый из которых пропорционален квадрату обобщенной координаты или импульса, то
членов, каждый из которых пропорционален квадрату обобщенной координаты или импульса, то
среднее значение  и
и

Измеренные значения  для инертных газов, которые, как известно, одноатомны, хорошо согласуются с этими классическими формулами при
для инертных газов, которые, как известно, одноатомны, хорошо согласуются с этими классическими формулами при  Кроме того, имеется несколько двухатомных газов, включая кислород и азот, для которых измеренные значения при «нормальных» температуре и давлении достаточно хорошо описываются этими формулами при
Кроме того, имеется несколько двухатомных газов, включая кислород и азот, для которых измеренные значения при «нормальных» температуре и давлении достаточно хорошо описываются этими формулами при  (например, для сухого воздуха при 15° С и атмосферном давлении измеренное значение у равно 1,4 с точностью до
(например, для сухого воздуха при 15° С и атмосферном давлении измеренное значение у равно 1,4 с точностью до  Однако во многих других случаях никакой выбор числа
Однако во многих других случаях никакой выбор числа  не приводит к хорошему соответствию с наблюдаемыми значениями теплоемкостей и часть внутренней энергии
не приводит к хорошему соответствию с наблюдаемыми значениями теплоемкостей и часть внутренней энергии  связанная с непоступательными движениями молекулы, очевидно, не всегда представляется в форме, даваемой классическими законами.
связанная с непоступательными движениями молекулы, очевидно, не всегда представляется в форме, даваемой классическими законами.
Известно, что зависимость удельной теплоемкости  от температуры
от температуры  для некоторых обычных многоатомных газов описывается кривой вроде изображенной на рис. 1.7.1 и ее можно получить с помощью квантовой механики. Величина энергии, связанной с непоступательными формами движения, квантуется и принимает одно из множества дискретных значений. Только когда величина
для некоторых обычных многоатомных газов описывается кривой вроде изображенной на рис. 1.7.1 и ее можно получить с помощью квантовой механики. Величина энергии, связанной с непоступательными формами движения, квантуется и принимает одно из множества дискретных значений. Только когда величина  значительно больше наименьшего из этих энергетических уровней, непрерывное распределение (1.7.4) дает удовлетворительное представление о равновесном состоянии газа, и только тогда средняя энергия, связанная с каждой формой движения, будет приближенно равна
значительно больше наименьшего из этих энергетических уровней, непрерывное распределение (1.7.4) дает удовлетворительное представление о равновесном состоянии газа, и только тогда средняя энергия, связанная с каждой формой движения, будет приближенно равна  При очень низких температурах газа ни одна из непоступательных форм движения молекулы не возбуждается и внутренняя энергия почти полностью является энергией поступательного движения, так что
При очень низких температурах газа ни одна из непоступательных форм движения молекулы не возбуждается и внутренняя энергия почти полностью является энергией поступательного движения, так что 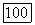 По мере возрастания температуры достигается наименьший энергетический уровень некоторой непоступательной формы движения, обычно вращательной формы, и функция
По мере возрастания температуры достигается наименьший энергетический уровень некоторой непоступательной формы движения, обычно вращательной формы, и функция 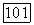 возрастает с температурой
возрастает с температурой 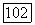 значительно быстрее, чем по линейному закону.
значительно быстрее, чем по линейному закону.
Плоский участок на графике рис. 1.7.1 соответствует промежуточному диапазону температур, таких, что величина 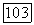 превосходит наименьший энергетический уровень вращательной формы движения настолько, чтобы энергия этой формы полностью входила в величину
превосходит наименьший энергетический уровень вращательной формы движения настолько, чтобы энергия этой формы полностью входила в величину 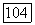 (т. е. была равна
(т. е. была равна 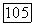 для двухатомных молекул), однако остается все еще намного меньше наименьшего энергетического уровня колебательных форм движения. Для воздуха энергия колебательных форм не имеет значения вплоть до температуры около 600° К, а теплоемкости
для двухатомных молекул), однако остается все еще намного меньше наименьшего энергетического уровня колебательных форм движения. Для воздуха энергия колебательных форм не имеет значения вплоть до температуры около 600° К, а теплоемкости 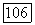 с достаточной
с достаточной

Рис. 1.7.1. Зависимость удельной теплоемкости газа от температуры для многоатомной молекулы.
точностью постоянны и равны соответственно 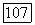 в диапазоне температур 250—400° К, который обычно включает «нормальные» температуры. При очень высоких температурах, свыше 20 000° К, значительная часть
в диапазоне температур 250—400° К, который обычно включает «нормальные» температуры. При очень высоких температурах, свыше 20 000° К, значительная часть 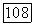 связана с энергией электронной системы молекулы (ее можно рассматривать как энергию вращения одноатомных молекул).
связана с энергией электронной системы молекулы (ее можно рассматривать как энергию вращения одноатомных молекул).
Для важного частного случая совершенного газа с постоянными удельными теплоемкостями (по крайней мере в некотором диапазоне температур), к которому близко подходит воздух при нормальных температуре и давлении, можно получить явные выражения для 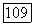 Вместо (1.7.20) можно записать
Вместо (1.7.20) можно записать

а из (1.7.21), используя уравнение состояния, находим

где постоянные 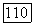 не имеют какого-либо абсолютного значения, если удельная теплоемкость
не имеют какого-либо абсолютного значения, если удельная теплоемкость 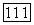 постоянна для всех температур, меньших
постоянна для всех температур, меньших 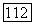 Из последней формулы следует связь между давлением
Из последней формулы следует связь между давлением 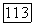 и плотностью
и плотностью 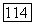 при изэнтропическом изменении состояния
при изэнтропическом изменении состояния

которое часто называют связью между давлением 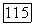 и плотностью
и плотностью 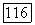 при адиабатическом изменении состояния совершенного газа, хотя для этого также необходимо, чтобы изменение состояния было обратимым (поскольку в противном случае энтропия
при адиабатическом изменении состояния совершенного газа, хотя для этого также необходимо, чтобы изменение состояния было обратимым (поскольку в противном случае энтропия 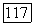 может не быть постоянной) и чтобы
может не быть постоянной) и чтобы 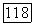 было постоянным.
было постоянным.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- ПРЕДИСЛОВИЕ
- 1. ФИЗИЧЕСКИЕ СВОЙСТВА ЖИДКОСТЕЙ
- 1.1. Твердые тела, жидкости и газы
- 1.2. Гипотеза сплошной среды
- 1.3. Объемные и поверхностные силы, действующие на жидкость
- 1.4. Механическое равновесие жидкости
- 1.5. Классическая термодинамика
- 1.6. Явления переноса
- Линейное соотношение между потоком и градиентом скалярной интенсивности
- Уравнения диффузии и теплопроводности в покоящейся изотропной среде
- Молекулярный перенос количества движения в жидкости
- 1.7. Отличительные свойства газов
- Отклонения от законов совершенного газа
- Коэффициенты переноса в совершенном газе
- Другие проявления отклонений совершенного газа от равновесного состояния
- 1.8. Отличительные свойства жидкостей
- Свойства жидкости в состоянии равновесия
- Коэффициенты переноса
- 1.9. Условия на границе между двумя средами
- Равновесная форма границы между двумя неподвижными, жидкостями
- Соотношения перехода на жидкой границе
- 2. КИНЕМАТИКА ПОЛЯ ТЕЧЕНИЯ
- Дифференцирование по направлению движения жидкости
- 2.2. Сохранение массы
- Использование функции тока для удовлетворения уравнения сохранения массы
- 2.3. Анализ относительного движения в окрестности точки
- Простое движение сдвига
- 2.4. Распределение скоростей при заданных скорости расширения и завихренности
- 2.5. Особенности скорости расширения. Источники и стоки
- 2.6. Распределение завихренности
- Вихревые нити
- Вихревая пелена
- 2.7. Распределения скорости при нулевой завихренности и нулевой скорости расширения
- Безвихревое соленоидалъное течение вблизи критической точки
- Комплексный потенциал двумерного безвихревого соленоидалъного течения
- 2.8. Безвихревое соленоидальное течение в двусвязных областях пространства
- Условия единственности для определения …
- 2.9. Трехмерные поля течения, простирающиеся в бесконечность
- Поведение потенциала на больших расстояниях
- Представление потенциала степенным рядом
- Безвихревое соленоидальное течение, вызываемое поступательным движением твердого тела
- 2.10. Двумерные поля течения, простирающиеся в бесконечность
- Безвихревое соленоидалъное течение, вызываемое поступательным движением твердого тела
- 3. УРАВНЕНИЯ ДВИЖЕНИЯ ЖИДКОСТИ
- Скорости изменения субстанциональных интегралов
- Законы сохранения для движущейся жидкости
- 3.2. Уравнение движения для жидкости
- Применение уравнения количества движения в интегральной форме
- Уравнения движения в подвижных осях
- 3.3. Выражение для тензора напряжений
- Механическое определение давления в движущейся жидкости
- Связь между девиатором напряжений и скоростью деформации для ньютоновой жидкости
- Условия для скорости и напряжений на жидкой границе двух сред
- 3.4. Изменение внутренней энергии движущейся жидкости
- 3.5. Теорема Бернулли для установившегося течения невязкой и нетеплопроводной жидкости
- Специальные формы теоремы Бернулли
- Сохранение величины Н при пересечении области перехода в одномерном установившемся течении
- 3.6. Полная система уравнений движения жидкости
- Изэнтпропическое течение
- Условия, при которых поле скоростей можно приближенно считать соленоидальным
- 3.7. Заключительные замечания к первым трем главам
- 4. РАВНОМЕРНЫЙ ПОТОК ВЯЗКОЙ НЕСЖИМАЕМОЙ ЖИДКОСТИ
- Модификация давления с учетом влияния массовой силы
- 4.2. Установившееся течение одного направления
- Течение Пуазейля
- Течение в трубах некругового поперечного сечения
- Двумерное течение
- Модель малярной кисти
- 4.3. Неустановившееся течение одного направления
- Плоская граница, внезапно приводимая в движение в покоящейся жидкости
- Твердая граница, внезапно приводимая в движение относительно другой неподвижной границы
- Течение, вызываемое колебанием плоской границы
- Начало течения в трубе
- 4.4. Слой Экмана на границе вращающейся жидкости
- Слой на свободной поверхности
- Слой на твердой плоской границе
- 4.5. Течение с круговыми линиями тока
- 4.6. Установившаяся струя из точечного источника количества движения
- 4.7. Динамическое подобие и число Рейнольдса
- Другие безразмерные параметры, имеющие динамическое значение
- 4.8. Поля течений, в которых силы инерции пренебрежимо малы
- Теория смазки
- Течение в приборе Хеле-Шоу
- Фильтрация через пористую среду
- Двумерное течение в угловой области
- Теоремы единственности и минимума диссипации энергии
- 4.9. Течение, вызываемое движением тела при малых числах Рейнольдса
- Сферическая капля в другой жидкости
- Тело произвольной формы
- 4.10. Уточненное уравнение Озеена для течения при малом числе Рейнольдса
- Твердая сфера
- Твердый круговой цилиндр
- 4.11. Вязкость разбавленной суспензии из малых частиц
- Сфера в чисто деформационном течении
- Повышенная скорость диссипации в несжимаемой суспензии
- Эффективная объемная вязкость жидкости, содержащей газовые пузырьки
- 4.12. Изменения в обтекании тел при возрастании числа Рейнольдса от 1 до 100
- 5. ТЕЧЕНИЕ ПРИ БОЛЬШОМ ЧИСЛЕ РЕЙНОЛЬДСА: ЭФФЕКТЫ ВЯЗКОСТИ
- Интенсификация завихренности при растяжении вихревых линий
- 5.3. Теорема Кельвина о циркуляции и законы распространения завихренности для невязкой жидкости
- Сохраняемость безвихревого движения
- 5.4. Возникновение завихренности при движениях жидкости из состояния покоя
- 5.5. Установившиеся течения, в которых диффузия завихренности, возникающей на твердой границе, ограничивается за счет конвекции
- (б) Течение в окрестности критической точки на твердой границе
- (в) Центробежное течение жидкости, вызванное вращающимся диском
- 5.6. Установившееся двумерное течение в сужающемся или расширяющемся канале
- Чисто сходящееся течение
- 5.7. Пограничные слои
- 5.8. Пограничный слой на плоской пластине
- 5.9. Эффекты ускорения и замедления внешнего потока
- Автомодельное решение, когда скорость внешнего течения пропорциональна x^m
- О расчетах установившегося пограничного слоя на движущемся в жидкости теле
- 5.10. Отрыв пограничного слоя
- 5.11. Течение при установившемся движении тел в жидкости
- Течение без отрыва пограничного слоя
- Течение с отрывом
- 5.12. Струи, свободные слои смешения и следы
- Свободные слои смешения
- Следы
- 5.13. Колеблющиеся пограничные слои
- Демпфирующая сила, действующая на колеблющееся тело
- Установившееся вторичное течение, обусловленное колеблющимся пограничным слоем
- Приложения теории установившегося вторичного течения
- 5.14. Течения со свободными поверхностями
- Сопротивление сферического газового пузырька при его установившемся всплывании в жидкости
- Затухание волн на поверхности тяжелой жидкости
- 5.15. Примеры применения теоремы о количестве движения
- Внезапное расширение трубы
- 6. ТЕОРИЯ БЕЗВИХРЕВОГО ТЕЧЕНИЯ И ЕЕ ПРИЛОЖЕНИЯ
- 6.2. Общие свойства безвихревого течения
- Интегрирование уравнения движения
- Выражения для кинетической энергии через интегралы по поверхности
- Теорема Кельвина о минимуме энергии
- Точки максимума скорости q и минимума давления р
- Локальное изменение величины скорости
- 6.3. Установившееся течение; некоторые приложения теоремы Бернулли и теоремы о количестве движения
- Истечение из круглого отверстия в открытом сосуде
- Водослив через плотину
- Удар струи жидкости о плоскую стенку
- 6.4. Общие свойства безвихревого течения, обусловленного движущимся твердым телом
- Кинетическая энергия жидкости
- Сила, действующая на тело при его поступательном движении
- Реакция на ускорение
- 6.5. Использование комплексного потенциала в случае двумерного безвихревого течения
- Конформное преобразование плоскости течения
- Преобразование границы в бесконечную прямую
- Теорема об окружности
- 6.6. Двумерное безвихревое течение, вызванное движущимся цилиндром с циркуляцией
- Поступательное движение эллиптического цилиндра
- Сила и момент, действующие на цилиндр в установившемся поступательном движении
- 6.7. Двумерные профили
- Возникновение циркуляции вокруг профиля и обоснование гипотезы Жуковского
- Профили, получаемые преобразованием окружности
- Профили Жуковского
- Движение системы точечных вихрей
- 6.8. Осесимметричное безвихревое течение, вызванное движением тела
- Движущаяся сфера
- Эллипсоиды вращения
- Тела, образуемые источниками на оси симметрии
- Полубесконечные тела
- 6.9. Приближенные результаты для тонких тел
- Тонкие тела в двух измерениях
- Тонкие профили в двух измерениях
- 6.10. Импульсивное движение жидкости
- Удар тела о свободную поверхность жидкости
- 6.11. Большие пузыри газа в жидкости
- Пузырь, поднимающийся в вертикальной трубе
- Расширяющийся сферический пузырь
- 6.12. Кавитация в жидкости
- Примеры образования каверн в неустановившемся течении
- Схлопывание нестационарной каверны
- Стационарные каверны
- 6.13. Теория течений со свободными линиями тока, установившиеся струи и каверны
- Двумерная струя, вытекающая на отверстия
- Двумерное обтекание пластины с каверной под давлением окружающей среды
- Стационарные каверны, присоединенные к телам в потоке жидкости
- 7. ВИХРЕВОЕ ТЕЧЕНИЕ ЭФФЕКТИВНО НЕВЯЗКОЙ ЖИДКОСТИ
- Самоиндуцированное движение вихревой нити
- 7.2. Течение неограниченной жидкости, покоящейся на бесконечности
- Полная кинетическая энергия жидкости
- Течение с круговыми вихревыми линиями
- Вихревые кольца
- 7.3. Двумерное течение неограниченной жидкости, покоящейся на бесконечности
- Интегральные инварианты распределения завихренности
- 7.4. Установившееся двумерное вихревое движение жидкости
- Постоянная завихренность в области, ограниченной снаружи
- Жидкость, вращающаяся на бесконечности как твердое тело
- Жидкость, совершающая в бесконечности простой сдвиг
- 7.5. Установившееся осесимметричное течение с закруткой
- Влияние изменения поперечного сечения трубы на течение закрученной жидкости
- Влияние изменения внешней скорости на изолированный вихрь
- 7.6. Жидкие системы, вращающиеся как целое
- Установившееся течение при малом числе Россби
- Распространение волн во вращающейся жидкости
- Течение, обусловленное движением тела вдоль оси вращения
- Геострофическое течение
- Течение над неровной поверхностью Земли
- Планетарные волны
- 7.8. Вихревая система крыла самолета
- Крылья большого относительного размаха и теория «несущей линии»
- Спутная вихревая система далеко за крылом
- Крылья с большой стреловидностью
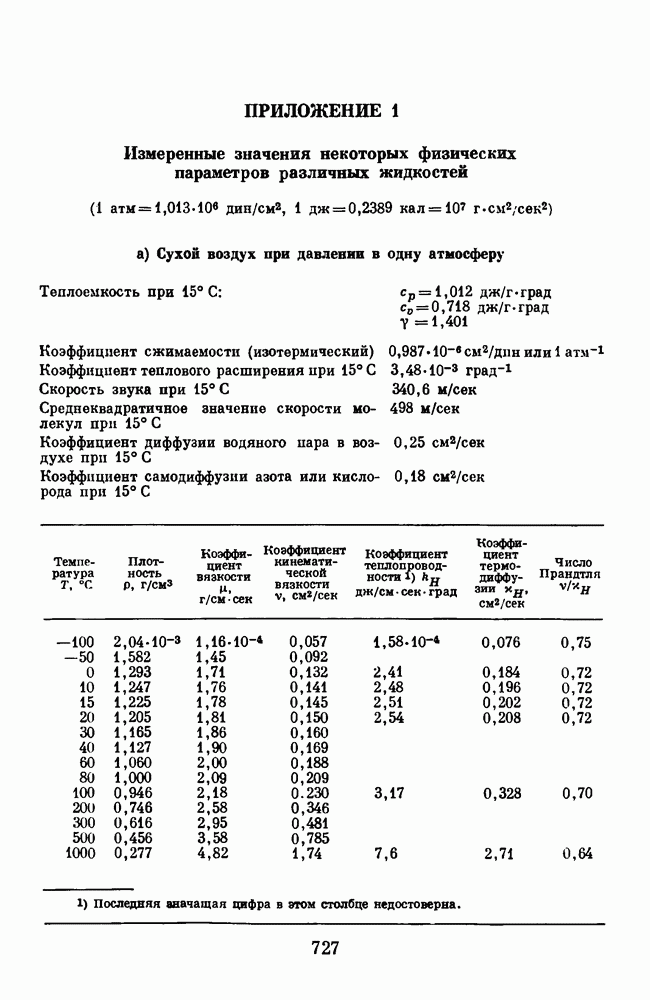
- ПРИЛОЖЕНИЕ 1. Измеренные значения некоторых физических параметров различных жидкостей
- ПРИЛОЖЕНИЕ 2. Выражения для некоторых векторных дифференциальных величин в ортогональных криволинейных координатах
- СПИСОК ЛИТЕРАТУРЫ