| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
Коэффициенты переноса в совершенном газе
Если некоторые параметры газа неоднородно распределены в пространстве и если эти параметры определяются величинами, которые связаны с отдельными молекулами и в некотором смысле сохраняются, то вследствие случайных движений молекул и неизменности их свойств с течением времени происходит сглаживание распределений параметров в пространстве. Явления молекулярного переноса подобного рода существуют у всех жидкостей, как уже отмечалось в § 1.6. В случае совершенного газа можно оценить величину коэффициентов переноса (представляемых параметрами  в выражении
в выражении  путем фактического расчета переноса, обусловленного молекулами, движущимися независимо друг от друга. Точный расчет коэффициентов переноса для газа сопряжен как с принципиальными, так и с математическими трудностями, и описание соответствующих методов и их результатов выходит за рамки данной книги.
путем фактического расчета переноса, обусловленного молекулами, движущимися независимо друг от друга. Точный расчет коэффициентов переноса для газа сопряжен как с принципиальными, так и с математическими трудностями, и описание соответствующих методов и их результатов выходит за рамки данной книги.
В совершенном газе, находящемся в состоянии равновесия, распределение молекул по скоростям (см. (1.7.8)) изотропно. Следовательно, реакция газа на отклонение от состояния равновесия в виде пространственной неоднородности параметров газа не имеет какого-либо предпочтительного направления, и поэтому тензор коэффициента переноса  определяется единственным скалярным параметром к, введенным в (1.6.2).
определяется единственным скалярным параметром к, введенным в (1.6.2).
Предположим, что неоднородность газа связана с некой величиной, которая в процессе столкновения молекул сохраняется и значение которой для данной молекулы равно  различные возможные интерпретации величины
различные возможные интерпретации величины  будут даны ниже. Тогда вследствие свободного перехода молекул с характеристикой
будут даны ниже. Тогда вследствие свободного перехода молекул с характеристикой  и скоростью и
и скоростью и  по нормали к элементу поверхности в газе происходит перенос этой величины (на единицу площади и в единицу времени), равной произведению и
по нормали к элементу поверхности в газе происходит перенос этой величины (на единицу площади и в единицу времени), равной произведению и  на число молекул в единице объема, и, таким образом, полный поток на единицу площади равен
на число молекул в единице объема, и, таким образом, полный поток на единицу площади равен

причем осреднение производится по всем молекулам в окрестности рассматриваемого элемента. Если локальная средняя (в том же самом смысле) величина  постоянна по всему газу, то статистически не может быть никаких данных, чтобы с определенным значением
постоянна по всему газу, то статистически не может быть никаких данных, чтобы с определенным значением  связать тот или иной знак нормальной скорости и
связать тот или иной знак нормальной скорости и  и поэтому полный поток равен нулю. С другой стороны, если величина
и поэтому полный поток равен нулю. С другой стороны, если величина  непостоянна, то молекулы, движущиеся в направлении возрастающих значений
непостоянна, то молекулы, движущиеся в направлении возрастающих значений  будут смешиваться с молекулами, имеющими величины
будут смешиваться с молекулами, имеющими величины  меньшие их локального среднего значения. Направление движения молекулы становится совершенно случайным в пределах нескольких столкновений после заданного направления движения, поэтому на поток может оказать влияние только изменение величины
меньшие их локального среднего значения. Направление движения молекулы становится совершенно случайным в пределах нескольких столкновений после заданного направления движения, поэтому на поток может оказать влияние только изменение величины  в пределах нескольких длин свободного пробега молекул от рассматриваемой точки; иначе говоря, поток может зависеть только от локального градиента величины
в пределах нескольких длин свободного пробега молекул от рассматриваемой точки; иначе говоря, поток может зависеть только от локального градиента величины  как и в более общем случае, обсуждавшемся в § 1.6.
как и в более общем случае, обсуждавшемся в § 1.6.
Если сделать грубое предположение, что в процессе свободного пробега молекула всегда имеет значение величины  равное
равное  в положении ее последнего столкновения, то значение
в положении ее последнего столкновения, то значение  на поверхности элемента определяется разностью
на поверхности элемента определяется разностью

где  вычислены при определенном положении элемента,
вычислены при определенном положении элемента,  промежуток времени, прошедший после столкновения. Еще одно грубое приближение, которое нужно сделать, заключается в том, что время
промежуток времени, прошедший после столкновения. Еще одно грубое приближение, которое нужно сделать, заключается в том, что время  можно заменить средним временем
можно заменить средним временем  между столкновениями. Тогда поток на единицу площади будет равен
между столкновениями. Тогда поток на единицу площади будет равен

В этом случае изотропной среды вектор потока  направлен вдоль локального градиента величины
направлен вдоль локального градиента величины  и поэтому величина вектора
и поэтому величина вектора  равна потоку на единицу площади через элемент поверхности с нормалью
равна потоку на единицу площади через элемент поверхности с нормалью  в направлении
в направлении  Отсюда следует выражение вектора потока
Отсюда следует выражение вектора потока

в котором мы пренебрегли малыми различиями среднеквадратичных значений компонент скорости и. Нельзя ожидать, что это выражение даст правильные численные результаты, но оно показывает, какие параметры влияют на коэффициенты переноса для совершенного газа. Характерным для этого выражения является произведение  которое входит в выражения всех коэффициентов Диффузии для совершенного газа. Можно написать произведение
которое входит в выражения всех коэффициентов Диффузии для совершенного газа. Можно написать произведение
 в виде
в виде  где I — некоторая средняя длина свободного пробега молекулы между столкновениями.
где I — некоторая средняя длина свободного пробега молекулы между столкновениями.
Придадим теперь величине  различные конкретные значения. Если
различные конкретные значения. Если  равно единице для молекул определенного вида и равно нулю для других молекул в смеси газов, то
равно единице для молекул определенного вида и равно нулю для других молекул в смеси газов, то  есть локально относительное количество отмеченных молекул, и оно совпадает с концентрацией С, введенной в § 1.6. Поток, определяемый выражением (1.7.27), представляет собой поток числа отмеченных молекул, и в этом случае выражение (1.7.27) эквивалентно оценке коэффициента диффузии
есть локально относительное количество отмеченных молекул, и оно совпадает с концентрацией С, введенной в § 1.6. Поток, определяемый выражением (1.7.27), представляет собой поток числа отмеченных молекул, и в этом случае выражение (1.7.27) эквивалентно оценке коэффициента диффузии  (см. (1.6.3) и (1.6.8)), который имеег порядок
(см. (1.6.3) и (1.6.8)), который имеег порядок  где
где  средние величины для отмеченных молекул. Величина
средние величины для отмеченных молекул. Величина  для отмеченных молекул может отличаться от ее значения для неотмеченных молекул, и она уменьшается с увеличением молекулярного веса отмеченных молекул в газе при данной температуре.
для отмеченных молекул может отличаться от ее значения для неотмеченных молекул, и она уменьшается с увеличением молекулярного веса отмеченных молекул в газе при данной температуре.
Если  есть полная энергия молекулы, то в этом случае отношение
есть полная энергия молекулы, то в этом случае отношение  представляет собой внутреннюю энергию единицы массы газа
представляет собой внутреннюю энергию единицы массы газа  и поток, определяемый выражением (1.7.27), есть по существу поток тепла. Поэтому на основании выражения (1.7.27) коэффициент теплопроводности
и поток, определяемый выражением (1.7.27), есть по существу поток тепла. Поэтому на основании выражения (1.7.27) коэффициент теплопроводности  определенный в § 1.6 как поток тепла через единицу площади на единицу локального градиента температуры
определенный в § 1.6 как поток тепла через единицу площади на единицу локального градиента температуры  знаком минус), имеет порядок
знаком минус), имеет порядок

и соответственно коэффициент термодиффузии  (см.
(см.  имеет порядок
имеет порядок 
Если в качестве  взять компоненту количества движения молекулы в данном направлении в плоскости элемента поверхности в газе, совершающем простое движение сдвига, так что скорость газа изменяется только в направлении нормали к элементу поверхности, то отношение
взять компоненту количества движения молекулы в данном направлении в плоскости элемента поверхности в газе, совершающем простое движение сдвига, так что скорость газа изменяется только в направлении нормали к элементу поверхности, то отношение  равно скорости газа
равно скорости газа  а поток, определяемый выражением (1.7.27) (которое, как предполагается в этом случае, применимо только лишь при одном выборе направления нормали к элементу поверхности), представляет собой касательную компоненту напряжения через элемент поверхности. Поэтому из выражения (1.7.27) можно установить, что коэффициент вязкости жидкости
а поток, определяемый выражением (1.7.27) (которое, как предполагается в этом случае, применимо только лишь при одном выборе направления нормали к элементу поверхности), представляет собой касательную компоненту напряжения через элемент поверхности. Поэтому из выражения (1.7.27) можно установить, что коэффициент вязкости жидкости  , определяемый равенством (1.6.15) как касательное напряжение, разделенное на градиент скорости жидкости,
, определяемый равенством (1.6.15) как касательное напряжение, разделенное на градиент скорости жидкости,
имеет порядок  а кинематический коэффициент вязкости
а кинематический коэффициент вязкости  он же коэффициент диффузии количества движения, имеет порядок
он же коэффициент диффузии количества движения, имеет порядок 
Оказывается, что для совершенного газа все три коэффициента диффузии имеют вид произведения

(хотя при диффузии одной из составных частей смеси величины  относятся к отмеченным молекулам, а не ко всему газу в целом). К сожалению, величины
относятся к отмеченным молекулам, а не ко всему газу в целом). К сожалению, величины  и I не вполне определены для реальных молекул, поскольку они требуют некоторого произвола при решении вопроса о том, что представляет собой столкновение молекул. Вследствие этого из предложенной выше простой теории нельзя априори сделать точные выводы об абсолютной величине рассматриваемых коэффициентов диффузии; в действительности более полезно действовать в обратном направлении и определять величины
и I не вполне определены для реальных молекул, поскольку они требуют некоторого произвола при решении вопроса о том, что представляет собой столкновение молекул. Вследствие этого из предложенной выше простой теории нельзя априори сделать точные выводы об абсолютной величине рассматриваемых коэффициентов диффузии; в действительности более полезно действовать в обратном направлении и определять величины  и I, используя теорию и наблюдаемые значения коэффициентов диффузии. Однако предсказание того, что коэффициенты диффузии отмеченных молекул (в случае самодиффузии), тепла и количества движения имеют одинаковый порядок величины, подтверждается опытом. Простая формула
и I, используя теорию и наблюдаемые значения коэффициентов диффузии. Однако предсказание того, что коэффициенты диффузии отмеченных молекул (в случае самодиффузии), тепла и количества движения имеют одинаковый порядок величины, подтверждается опытом. Простая формула

хорошо согласуется с измерениями кинематического коэффициента вязкости  и коэффициента диффузии
и коэффициента диффузии  для многих газов. Для воздуха эта формула дает
для многих газов. Для воздуха эта формула дает  при наблюдаемом значении 0.72. Измерениями установлено, что отношение
при наблюдаемом значении 0.72. Измерениями установлено, что отношение  коэффициент самодиффузии) находится для большинства простых газов между 0,6 и 0,8.
коэффициент самодиффузии) находится для большинства простых газов между 0,6 и 0,8.
Представляет интерес также зависимость коэффициентов диффузии от абсолютной температуры и плотности, устанавливаемая оценкой (1.7.28). Средняя величина  зависит только от температуры
зависит только от температуры  и изменяется по
и изменяется по  линейно. При данной температуре и, следовательно, при данном типе столкновений количество молекул в каждый момент времени в цилиндре единичной длины, который условно проходит молекула при ее свободном движении, пропорционально
линейно. При данной температуре и, следовательно, при данном типе столкновений количество молекул в каждый момент времени в цилиндре единичной длины, который условно проходит молекула при ее свободном движении, пропорционально  так что произведение
так что произведение  постоянно; по мере же увеличения температуры
постоянно; по мере же увеличения температуры  (и средней скорости молекул) можно ожидать небольшого уменьшения эффективного числа столкновений молекулы на единице длины пробега, поскольку более
(и средней скорости молекул) можно ожидать небольшого уменьшения эффективного числа столкновений молекулы на единице длины пробега, поскольку более
отдаленные встречи молекул друг с другом уже нельзя будет считать столкновениями. Следовательно, должно быть

где величина а учитывает влияние температуры на процессы столкновения и, как показали наблюдения, для воздуха в диапазоне температур 200—400° К она приблизительно равна 0,25.
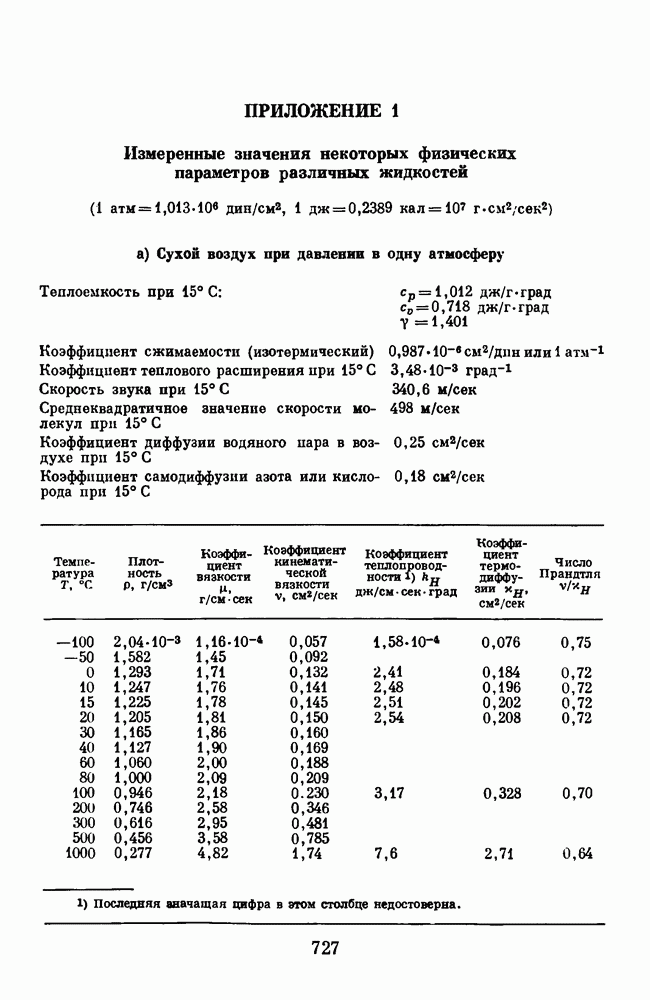
Измеренные значения коэффициентов диффузии и других параметров для воздуха при различных значениях температуры  и плотности
и плотности  приведены в приложении 1 в конце книги.
приведены в приложении 1 в конце книги.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- ПРЕДИСЛОВИЕ
- 1. ФИЗИЧЕСКИЕ СВОЙСТВА ЖИДКОСТЕЙ
- 1.1. Твердые тела, жидкости и газы
- 1.2. Гипотеза сплошной среды
- 1.3. Объемные и поверхностные силы, действующие на жидкость
- 1.4. Механическое равновесие жидкости
- 1.5. Классическая термодинамика
- 1.6. Явления переноса
- Линейное соотношение между потоком и градиентом скалярной интенсивности
- Уравнения диффузии и теплопроводности в покоящейся изотропной среде
- Молекулярный перенос количества движения в жидкости
- 1.7. Отличительные свойства газов
- Отклонения от законов совершенного газа
- Коэффициенты переноса в совершенном газе
- Другие проявления отклонений совершенного газа от равновесного состояния
- 1.8. Отличительные свойства жидкостей
- Свойства жидкости в состоянии равновесия
- Коэффициенты переноса
- 1.9. Условия на границе между двумя средами
- Равновесная форма границы между двумя неподвижными, жидкостями
- Соотношения перехода на жидкой границе
- 2. КИНЕМАТИКА ПОЛЯ ТЕЧЕНИЯ
- Дифференцирование по направлению движения жидкости
- 2.2. Сохранение массы
- Использование функции тока для удовлетворения уравнения сохранения массы
- 2.3. Анализ относительного движения в окрестности точки
- Простое движение сдвига
- 2.4. Распределение скоростей при заданных скорости расширения и завихренности
- 2.5. Особенности скорости расширения. Источники и стоки
- 2.6. Распределение завихренности
- Вихревые нити
- Вихревая пелена
- 2.7. Распределения скорости при нулевой завихренности и нулевой скорости расширения
- Безвихревое соленоидалъное течение вблизи критической точки
- Комплексный потенциал двумерного безвихревого соленоидалъного течения
- 2.8. Безвихревое соленоидальное течение в двусвязных областях пространства
- Условия единственности для определения …
- 2.9. Трехмерные поля течения, простирающиеся в бесконечность
- Поведение потенциала на больших расстояниях
- Представление потенциала степенным рядом
- Безвихревое соленоидальное течение, вызываемое поступательным движением твердого тела
- 2.10. Двумерные поля течения, простирающиеся в бесконечность
- Безвихревое соленоидалъное течение, вызываемое поступательным движением твердого тела
- 3. УРАВНЕНИЯ ДВИЖЕНИЯ ЖИДКОСТИ
- Скорости изменения субстанциональных интегралов
- Законы сохранения для движущейся жидкости
- 3.2. Уравнение движения для жидкости
- Применение уравнения количества движения в интегральной форме
- Уравнения движения в подвижных осях
- 3.3. Выражение для тензора напряжений
- Механическое определение давления в движущейся жидкости
- Связь между девиатором напряжений и скоростью деформации для ньютоновой жидкости
- Условия для скорости и напряжений на жидкой границе двух сред
- 3.4. Изменение внутренней энергии движущейся жидкости
- 3.5. Теорема Бернулли для установившегося течения невязкой и нетеплопроводной жидкости
- Специальные формы теоремы Бернулли
- Сохранение величины Н при пересечении области перехода в одномерном установившемся течении
- 3.6. Полная система уравнений движения жидкости
- Изэнтпропическое течение
- Условия, при которых поле скоростей можно приближенно считать соленоидальным
- 3.7. Заключительные замечания к первым трем главам
- 4. РАВНОМЕРНЫЙ ПОТОК ВЯЗКОЙ НЕСЖИМАЕМОЙ ЖИДКОСТИ
- Модификация давления с учетом влияния массовой силы
- 4.2. Установившееся течение одного направления
- Течение Пуазейля
- Течение в трубах некругового поперечного сечения
- Двумерное течение
- Модель малярной кисти
- 4.3. Неустановившееся течение одного направления
- Плоская граница, внезапно приводимая в движение в покоящейся жидкости
- Твердая граница, внезапно приводимая в движение относительно другой неподвижной границы
- Течение, вызываемое колебанием плоской границы
- Начало течения в трубе
- 4.4. Слой Экмана на границе вращающейся жидкости
- Слой на свободной поверхности
- Слой на твердой плоской границе
- 4.5. Течение с круговыми линиями тока
- 4.6. Установившаяся струя из точечного источника количества движения
- 4.7. Динамическое подобие и число Рейнольдса
- Другие безразмерные параметры, имеющие динамическое значение
- 4.8. Поля течений, в которых силы инерции пренебрежимо малы
- Теория смазки
- Течение в приборе Хеле-Шоу
- Фильтрация через пористую среду
- Двумерное течение в угловой области
- Теоремы единственности и минимума диссипации энергии
- 4.9. Течение, вызываемое движением тела при малых числах Рейнольдса
- Сферическая капля в другой жидкости
- Тело произвольной формы
- 4.10. Уточненное уравнение Озеена для течения при малом числе Рейнольдса
- Твердая сфера
- Твердый круговой цилиндр
- 4.11. Вязкость разбавленной суспензии из малых частиц
- Сфера в чисто деформационном течении
- Повышенная скорость диссипации в несжимаемой суспензии
- Эффективная объемная вязкость жидкости, содержащей газовые пузырьки
- 4.12. Изменения в обтекании тел при возрастании числа Рейнольдса от 1 до 100
- 5. ТЕЧЕНИЕ ПРИ БОЛЬШОМ ЧИСЛЕ РЕЙНОЛЬДСА: ЭФФЕКТЫ ВЯЗКОСТИ
- Интенсификация завихренности при растяжении вихревых линий
- 5.3. Теорема Кельвина о циркуляции и законы распространения завихренности для невязкой жидкости
- Сохраняемость безвихревого движения
- 5.4. Возникновение завихренности при движениях жидкости из состояния покоя
- 5.5. Установившиеся течения, в которых диффузия завихренности, возникающей на твердой границе, ограничивается за счет конвекции
- (б) Течение в окрестности критической точки на твердой границе
- (в) Центробежное течение жидкости, вызванное вращающимся диском
- 5.6. Установившееся двумерное течение в сужающемся или расширяющемся канале
- Чисто сходящееся течение
- 5.7. Пограничные слои
- 5.8. Пограничный слой на плоской пластине
- 5.9. Эффекты ускорения и замедления внешнего потока
- Автомодельное решение, когда скорость внешнего течения пропорциональна x^m
- О расчетах установившегося пограничного слоя на движущемся в жидкости теле
- 5.10. Отрыв пограничного слоя
- 5.11. Течение при установившемся движении тел в жидкости
- Течение без отрыва пограничного слоя
- Течение с отрывом
- 5.12. Струи, свободные слои смешения и следы
- Свободные слои смешения
- Следы
- 5.13. Колеблющиеся пограничные слои
- Демпфирующая сила, действующая на колеблющееся тело
- Установившееся вторичное течение, обусловленное колеблющимся пограничным слоем
- Приложения теории установившегося вторичного течения
- 5.14. Течения со свободными поверхностями
- Сопротивление сферического газового пузырька при его установившемся всплывании в жидкости
- Затухание волн на поверхности тяжелой жидкости
- 5.15. Примеры применения теоремы о количестве движения
- Внезапное расширение трубы
- 6. ТЕОРИЯ БЕЗВИХРЕВОГО ТЕЧЕНИЯ И ЕЕ ПРИЛОЖЕНИЯ
- 6.2. Общие свойства безвихревого течения
- Интегрирование уравнения движения
- Выражения для кинетической энергии через интегралы по поверхности
- Теорема Кельвина о минимуме энергии
- Точки максимума скорости q и минимума давления р
- Локальное изменение величины скорости
- 6.3. Установившееся течение; некоторые приложения теоремы Бернулли и теоремы о количестве движения
- Истечение из круглого отверстия в открытом сосуде
- Водослив через плотину
- Удар струи жидкости о плоскую стенку
- 6.4. Общие свойства безвихревого течения, обусловленного движущимся твердым телом
- Кинетическая энергия жидкости
- Сила, действующая на тело при его поступательном движении
- Реакция на ускорение
- 6.5. Использование комплексного потенциала в случае двумерного безвихревого течения
- Конформное преобразование плоскости течения
- Преобразование границы в бесконечную прямую
- Теорема об окружности
- 6.6. Двумерное безвихревое течение, вызванное движущимся цилиндром с циркуляцией
- Поступательное движение эллиптического цилиндра
- Сила и момент, действующие на цилиндр в установившемся поступательном движении
- 6.7. Двумерные профили
- Возникновение циркуляции вокруг профиля и обоснование гипотезы Жуковского
- Профили, получаемые преобразованием окружности
- Профили Жуковского
- Движение системы точечных вихрей
- 6.8. Осесимметричное безвихревое течение, вызванное движением тела
- Движущаяся сфера
- Эллипсоиды вращения
- Тела, образуемые источниками на оси симметрии
- Полубесконечные тела
- 6.9. Приближенные результаты для тонких тел
- Тонкие тела в двух измерениях
- Тонкие профили в двух измерениях
- 6.10. Импульсивное движение жидкости
- Удар тела о свободную поверхность жидкости
- 6.11. Большие пузыри газа в жидкости
- Пузырь, поднимающийся в вертикальной трубе
- Расширяющийся сферический пузырь
- 6.12. Кавитация в жидкости
- Примеры образования каверн в неустановившемся течении
- Схлопывание нестационарной каверны
- Стационарные каверны
- 6.13. Теория течений со свободными линиями тока, установившиеся струи и каверны
- Двумерная струя, вытекающая на отверстия
- Двумерное обтекание пластины с каверной под давлением окружающей среды
- Стационарные каверны, присоединенные к телам в потоке жидкости
- 7. ВИХРЕВОЕ ТЕЧЕНИЕ ЭФФЕКТИВНО НЕВЯЗКОЙ ЖИДКОСТИ
- Самоиндуцированное движение вихревой нити
- 7.2. Течение неограниченной жидкости, покоящейся на бесконечности
- Полная кинетическая энергия жидкости
- Течение с круговыми вихревыми линиями
- Вихревые кольца
- 7.3. Двумерное течение неограниченной жидкости, покоящейся на бесконечности
- Интегральные инварианты распределения завихренности
- 7.4. Установившееся двумерное вихревое движение жидкости
- Постоянная завихренность в области, ограниченной снаружи
- Жидкость, вращающаяся на бесконечности как твердое тело
- Жидкость, совершающая в бесконечности простой сдвиг
- 7.5. Установившееся осесимметричное течение с закруткой
- Влияние изменения поперечного сечения трубы на течение закрученной жидкости
- Влияние изменения внешней скорости на изолированный вихрь
- 7.6. Жидкие системы, вращающиеся как целое
- Установившееся течение при малом числе Россби
- Распространение волн во вращающейся жидкости
- Течение, обусловленное движением тела вдоль оси вращения
- Геострофическое течение
- Течение над неровной поверхностью Земли
- Планетарные волны
- 7.8. Вихревая система крыла самолета
- Крылья большого относительного размаха и теория «несущей линии»
- Спутная вихревая система далеко за крылом
- Крылья с большой стреловидностью
- ПРИЛОЖЕНИЕ 1. Измеренные значения некоторых физических параметров различных жидкостей
- ПРИЛОЖЕНИЕ 2. Выражения для некоторых векторных дифференциальных величин в ортогональных криволинейных координатах
- СПИСОК ЛИТЕРАТУРЫ