| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
1.8. Отличительные свойства жидкостей
О строении жидкостей известно значительно меньше, чем о строении газов. Для вывода приближенных результатов применительно к жидкостям не имеется никакой простой модели, подобной модели совершенного газа с динамически независимыми молекулами. Вследствие этого невозможно логически установить многие из наблюдаемых свойств жидкости или объяснить их через свойства отдельных молекул. Еще одна помеха заключается в том, что вода, которая представляет собой частную жидкость исключительно большого практического значения, обладает многими аномальными свойствами. В этом параграфе многие известные динамические свойства обычных жидкостей будут описаны без особых пояснений. В частности, численные значения некоторых физических параметров для чистой воды приведены в конце книги в приложении 1.
Основное свойство жидких и твердых фаз состоит в том, что они являются конденсированными фазами, в которых каждая молекула все время находится под действием интенсивных сил сцепления соседних с ней молекул. Однако жидкости обладают общим с газами свойством текучести и способностью к свободному изменению формы. В однородной покоящейся жидкости точно так же, как и в газе, касательные компоненты напряжения равны нулю, работа, совершаемая над единицей массы жидкости при медленном изменении ее плотности на малую величину  равна
равна  и уравнение состояния связывает три переменные
и уравнение состояния связывает три переменные  и
и 
Данное вещество может существовать в жидкой фазе при некоторых значениях двух параметров состояния (например,  и
и 

Рис. 1.8.1. Изотермы типичных парожидкостных систем. 1 — изотермы; 2 — жидкая фаза; 3 — критическая точка; 4 — область двухфазного состояния; 5 — паровая фаза.
и в газообразной фазе при других значениях этих параметров. Причина существования двух различных фаз жидкости с существенно разными значениями плотности связана, конечно, с изменением межмолекулярной силы при изменении расстояния между молекулами. Если масса газа изотермически сжимается, то средняя энергия поступательного движения молекулы остается постоянной, а среднее расстояние между соседними молекулами уменьшается. Когда удельный объем газа настолько мал, что среднее расстояние между молекулами равно всего нескольким их диаметрам, силы притяжения между молекулами становятся значительными и давление, развиваемое газом, становится меньше потока нормальной компоненты количества движения, определяемой равенством (1.7.1). Если температура меньше критической  то дальнейшее уменьшение удельного объема приводит к неустойчивому состоянию, в котором молекулы не могут избежать влияния сил притяжения соседних молекул, и появляются центры конденсации молекул. Образование нескольких таких центров плотно упакованных молекул уменьшает числовую плотность молекул, все еще движущихся свободно и независимо друг от друга, так что при данной общей плотности устанавливается новое равновесие, в котором определенная (средняя) часть массы находится в конденсированной (жидкой) фазе, а остальная — в дисперсной или паровой фазе. Такое многофазное равновесие весьма чувствительно к изменениям давления; небольшое увеличение давления приводит к полностью конденсированной однородной жидкой
то дальнейшее уменьшение удельного объема приводит к неустойчивому состоянию, в котором молекулы не могут избежать влияния сил притяжения соседних молекул, и появляются центры конденсации молекул. Образование нескольких таких центров плотно упакованных молекул уменьшает числовую плотность молекул, все еще движущихся свободно и независимо друг от друга, так что при данной общей плотности устанавливается новое равновесие, в котором определенная (средняя) часть массы находится в конденсированной (жидкой) фазе, а остальная — в дисперсной или паровой фазе. Такое многофазное равновесие весьма чувствительно к изменениям давления; небольшое увеличение давления приводит к полностью конденсированной однородной жидкой
фазе с большой плотностью, а малое уменьшение давления приводит к однородной паровой фазе со значительно меньшей плотностью.
Изотермы на диаграмме состояний для типичной системы жидкость — пар изображены на рис. 1.8.1. Приблизительно постоянное давление на изотерме, проходящей через многофазную область, называется давлением насыщенного пара  т. е. давлением, существующим в чистом паре, который граничит с жидкостью при данной температуре. При температурах выше критической
т. е. давлением, существующим в чистом паре, который граничит с жидкостью при данной температуре. При температурах выше критической  энергия поступательного движения молекул оказывается достаточно большой, чтобы помешать образованию центров конденсации молекул, и существует непрерывный переход вдоль изотермы от вещества со свойствами, близкими к газу при малых плотностях, к веществу со свойствами, похожими на свойства жидкостей при больших плотностях. Уравнение состояния Ван-дер-Ваальса (1.7.26) качественно воспроизводит основные свойства наблюдаемых изотерм, но, как уже отмечалось, оно не выполняется, если вещество находится в конденсированной фазе или близко к состоянию конденсации.
энергия поступательного движения молекул оказывается достаточно большой, чтобы помешать образованию центров конденсации молекул, и существует непрерывный переход вдоль изотермы от вещества со свойствами, близкими к газу при малых плотностях, к веществу со свойствами, похожими на свойства жидкостей при больших плотностях. Уравнение состояния Ван-дер-Ваальса (1.7.26) качественно воспроизводит основные свойства наблюдаемых изотерм, но, как уже отмечалось, оно не выполняется, если вещество находится в конденсированной фазе или близко к состоянию конденсации.
Для воды Тк  а давление и плотность в точке, где критическая изотерма касается области многофазного состояния вещества (в критической точке), равны соответственно 218 атм и около
а давление и плотность в точке, где критическая изотерма касается области многофазного состояния вещества (в критической точке), равны соответственно 218 атм и около  Изотерма, соответствующая нормальной температуре
Изотерма, соответствующая нормальной температуре  идет почти горизонтально через многофазную область при давлении
идет почти горизонтально через многофазную область при давлении  , или 0,017 атм, и пересекает границы многофазной области при плотностях
, или 0,017 атм, и пересекает границы многофазной области при плотностях  (однородная жидкость) и
(однородная жидкость) и  (однородный пар); следовательно, жидкая и газообразная фазы воды при нормальной температуре совершенно различны.
(однородный пар); следовательно, жидкая и газообразная фазы воды при нормальной температуре совершенно различны.
Эффект уменьшения давления ниже давления насыщенного пара имеет особое значение в механике жидкости, поскольку изменения давлений в потоке воды (которые более вероятно считать адиабатическими, а не изотермическими) могут легко превысить одну атмосферу. Когда давление в жидкости уменьшается до значения, незначительно отличающегося от давления насыщенного пара при температуре жидкости, она оказывается в неустойчивом состоянии и, как правило, в жидкости появляются полости, заполненные паром.
Процесс появления таких полостей, называемый кавитацией, приводит к важным механическим следствиям в потоке жидкости, которые будут рассмотрены в § 6.12 и 6.13.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- ПРЕДИСЛОВИЕ
- 1. ФИЗИЧЕСКИЕ СВОЙСТВА ЖИДКОСТЕЙ
- 1.1. Твердые тела, жидкости и газы
- 1.2. Гипотеза сплошной среды
- 1.3. Объемные и поверхностные силы, действующие на жидкость
- 1.4. Механическое равновесие жидкости
- 1.5. Классическая термодинамика
- 1.6. Явления переноса
- Линейное соотношение между потоком и градиентом скалярной интенсивности
- Уравнения диффузии и теплопроводности в покоящейся изотропной среде
- Молекулярный перенос количества движения в жидкости
- 1.7. Отличительные свойства газов
- Отклонения от законов совершенного газа
- Коэффициенты переноса в совершенном газе
- Другие проявления отклонений совершенного газа от равновесного состояния
- 1.8. Отличительные свойства жидкостей
- Свойства жидкости в состоянии равновесия
- Коэффициенты переноса
- 1.9. Условия на границе между двумя средами
- Равновесная форма границы между двумя неподвижными, жидкостями
- Соотношения перехода на жидкой границе
- 2. КИНЕМАТИКА ПОЛЯ ТЕЧЕНИЯ
- Дифференцирование по направлению движения жидкости
- 2.2. Сохранение массы
- Использование функции тока для удовлетворения уравнения сохранения массы
- 2.3. Анализ относительного движения в окрестности точки
- Простое движение сдвига
- 2.4. Распределение скоростей при заданных скорости расширения и завихренности
- 2.5. Особенности скорости расширения. Источники и стоки
- 2.6. Распределение завихренности
- Вихревые нити
- Вихревая пелена
- 2.7. Распределения скорости при нулевой завихренности и нулевой скорости расширения
- Безвихревое соленоидалъное течение вблизи критической точки
- Комплексный потенциал двумерного безвихревого соленоидалъного течения
- 2.8. Безвихревое соленоидальное течение в двусвязных областях пространства
- Условия единственности для определения …
- 2.9. Трехмерные поля течения, простирающиеся в бесконечность
- Поведение потенциала на больших расстояниях
- Представление потенциала степенным рядом
- Безвихревое соленоидальное течение, вызываемое поступательным движением твердого тела
- 2.10. Двумерные поля течения, простирающиеся в бесконечность
- Безвихревое соленоидалъное течение, вызываемое поступательным движением твердого тела
- 3. УРАВНЕНИЯ ДВИЖЕНИЯ ЖИДКОСТИ
- Скорости изменения субстанциональных интегралов
- Законы сохранения для движущейся жидкости
- 3.2. Уравнение движения для жидкости
- Применение уравнения количества движения в интегральной форме
- Уравнения движения в подвижных осях
- 3.3. Выражение для тензора напряжений
- Механическое определение давления в движущейся жидкости
- Связь между девиатором напряжений и скоростью деформации для ньютоновой жидкости
- Условия для скорости и напряжений на жидкой границе двух сред
- 3.4. Изменение внутренней энергии движущейся жидкости
- 3.5. Теорема Бернулли для установившегося течения невязкой и нетеплопроводной жидкости
- Специальные формы теоремы Бернулли
- Сохранение величины Н при пересечении области перехода в одномерном установившемся течении
- 3.6. Полная система уравнений движения жидкости
- Изэнтпропическое течение
- Условия, при которых поле скоростей можно приближенно считать соленоидальным
- 3.7. Заключительные замечания к первым трем главам
- 4. РАВНОМЕРНЫЙ ПОТОК ВЯЗКОЙ НЕСЖИМАЕМОЙ ЖИДКОСТИ
- Модификация давления с учетом влияния массовой силы
- 4.2. Установившееся течение одного направления
- Течение Пуазейля
- Течение в трубах некругового поперечного сечения
- Двумерное течение
- Модель малярной кисти
- 4.3. Неустановившееся течение одного направления
- Плоская граница, внезапно приводимая в движение в покоящейся жидкости
- Твердая граница, внезапно приводимая в движение относительно другой неподвижной границы
- Течение, вызываемое колебанием плоской границы
- Начало течения в трубе
- 4.4. Слой Экмана на границе вращающейся жидкости
- Слой на свободной поверхности
- Слой на твердой плоской границе
- 4.5. Течение с круговыми линиями тока
- 4.6. Установившаяся струя из точечного источника количества движения
- 4.7. Динамическое подобие и число Рейнольдса
- Другие безразмерные параметры, имеющие динамическое значение
- 4.8. Поля течений, в которых силы инерции пренебрежимо малы
- Теория смазки
- Течение в приборе Хеле-Шоу
- Фильтрация через пористую среду
- Двумерное течение в угловой области
- Теоремы единственности и минимума диссипации энергии
- 4.9. Течение, вызываемое движением тела при малых числах Рейнольдса
- Сферическая капля в другой жидкости
- Тело произвольной формы
- 4.10. Уточненное уравнение Озеена для течения при малом числе Рейнольдса
- Твердая сфера
- Твердый круговой цилиндр
- 4.11. Вязкость разбавленной суспензии из малых частиц
- Сфера в чисто деформационном течении
- Повышенная скорость диссипации в несжимаемой суспензии
- Эффективная объемная вязкость жидкости, содержащей газовые пузырьки
- 4.12. Изменения в обтекании тел при возрастании числа Рейнольдса от 1 до 100
- 5. ТЕЧЕНИЕ ПРИ БОЛЬШОМ ЧИСЛЕ РЕЙНОЛЬДСА: ЭФФЕКТЫ ВЯЗКОСТИ
- Интенсификация завихренности при растяжении вихревых линий
- 5.3. Теорема Кельвина о циркуляции и законы распространения завихренности для невязкой жидкости
- Сохраняемость безвихревого движения
- 5.4. Возникновение завихренности при движениях жидкости из состояния покоя
- 5.5. Установившиеся течения, в которых диффузия завихренности, возникающей на твердой границе, ограничивается за счет конвекции
- (б) Течение в окрестности критической точки на твердой границе
- (в) Центробежное течение жидкости, вызванное вращающимся диском
- 5.6. Установившееся двумерное течение в сужающемся или расширяющемся канале
- Чисто сходящееся течение
- 5.7. Пограничные слои
- 5.8. Пограничный слой на плоской пластине
- 5.9. Эффекты ускорения и замедления внешнего потока
- Автомодельное решение, когда скорость внешнего течения пропорциональна x^m
- О расчетах установившегося пограничного слоя на движущемся в жидкости теле
- 5.10. Отрыв пограничного слоя
- 5.11. Течение при установившемся движении тел в жидкости
- Течение без отрыва пограничного слоя
- Течение с отрывом
- 5.12. Струи, свободные слои смешения и следы
- Свободные слои смешения
- Следы
- 5.13. Колеблющиеся пограничные слои
- Демпфирующая сила, действующая на колеблющееся тело
- Установившееся вторичное течение, обусловленное колеблющимся пограничным слоем
- Приложения теории установившегося вторичного течения
- 5.14. Течения со свободными поверхностями
- Сопротивление сферического газового пузырька при его установившемся всплывании в жидкости
- Затухание волн на поверхности тяжелой жидкости
- 5.15. Примеры применения теоремы о количестве движения
- Внезапное расширение трубы
- 6. ТЕОРИЯ БЕЗВИХРЕВОГО ТЕЧЕНИЯ И ЕЕ ПРИЛОЖЕНИЯ
- 6.2. Общие свойства безвихревого течения
- Интегрирование уравнения движения
- Выражения для кинетической энергии через интегралы по поверхности
- Теорема Кельвина о минимуме энергии
- Точки максимума скорости q и минимума давления р
- Локальное изменение величины скорости
- 6.3. Установившееся течение; некоторые приложения теоремы Бернулли и теоремы о количестве движения
- Истечение из круглого отверстия в открытом сосуде
- Водослив через плотину
- Удар струи жидкости о плоскую стенку
- 6.4. Общие свойства безвихревого течения, обусловленного движущимся твердым телом
- Кинетическая энергия жидкости
- Сила, действующая на тело при его поступательном движении
- Реакция на ускорение
- 6.5. Использование комплексного потенциала в случае двумерного безвихревого течения
- Конформное преобразование плоскости течения
- Преобразование границы в бесконечную прямую
- Теорема об окружности
- 6.6. Двумерное безвихревое течение, вызванное движущимся цилиндром с циркуляцией
- Поступательное движение эллиптического цилиндра
- Сила и момент, действующие на цилиндр в установившемся поступательном движении
- 6.7. Двумерные профили
- Возникновение циркуляции вокруг профиля и обоснование гипотезы Жуковского
- Профили, получаемые преобразованием окружности
- Профили Жуковского
- Движение системы точечных вихрей
- 6.8. Осесимметричное безвихревое течение, вызванное движением тела
- Движущаяся сфера
- Эллипсоиды вращения
- Тела, образуемые источниками на оси симметрии
- Полубесконечные тела
- 6.9. Приближенные результаты для тонких тел
- Тонкие тела в двух измерениях
- Тонкие профили в двух измерениях
- 6.10. Импульсивное движение жидкости
- Удар тела о свободную поверхность жидкости
- 6.11. Большие пузыри газа в жидкости
- Пузырь, поднимающийся в вертикальной трубе
- Расширяющийся сферический пузырь
- 6.12. Кавитация в жидкости
- Примеры образования каверн в неустановившемся течении
- Схлопывание нестационарной каверны
- Стационарные каверны
- 6.13. Теория течений со свободными линиями тока, установившиеся струи и каверны
- Двумерная струя, вытекающая на отверстия
- Двумерное обтекание пластины с каверной под давлением окружающей среды
- Стационарные каверны, присоединенные к телам в потоке жидкости
- 7. ВИХРЕВОЕ ТЕЧЕНИЕ ЭФФЕКТИВНО НЕВЯЗКОЙ ЖИДКОСТИ
- Самоиндуцированное движение вихревой нити
- 7.2. Течение неограниченной жидкости, покоящейся на бесконечности
- Полная кинетическая энергия жидкости
- Течение с круговыми вихревыми линиями
- Вихревые кольца
- 7.3. Двумерное течение неограниченной жидкости, покоящейся на бесконечности
- Интегральные инварианты распределения завихренности
- 7.4. Установившееся двумерное вихревое движение жидкости
- Постоянная завихренность в области, ограниченной снаружи
- Жидкость, вращающаяся на бесконечности как твердое тело
- Жидкость, совершающая в бесконечности простой сдвиг
- 7.5. Установившееся осесимметричное течение с закруткой
- Влияние изменения поперечного сечения трубы на течение закрученной жидкости
- Влияние изменения внешней скорости на изолированный вихрь
- 7.6. Жидкие системы, вращающиеся как целое
- Установившееся течение при малом числе Россби
- Распространение волн во вращающейся жидкости
- Течение, обусловленное движением тела вдоль оси вращения
- Геострофическое течение
- Течение над неровной поверхностью Земли
- Планетарные волны
- 7.8. Вихревая система крыла самолета
- Крылья большого относительного размаха и теория «несущей линии»
- Спутная вихревая система далеко за крылом
- Крылья с большой стреловидностью
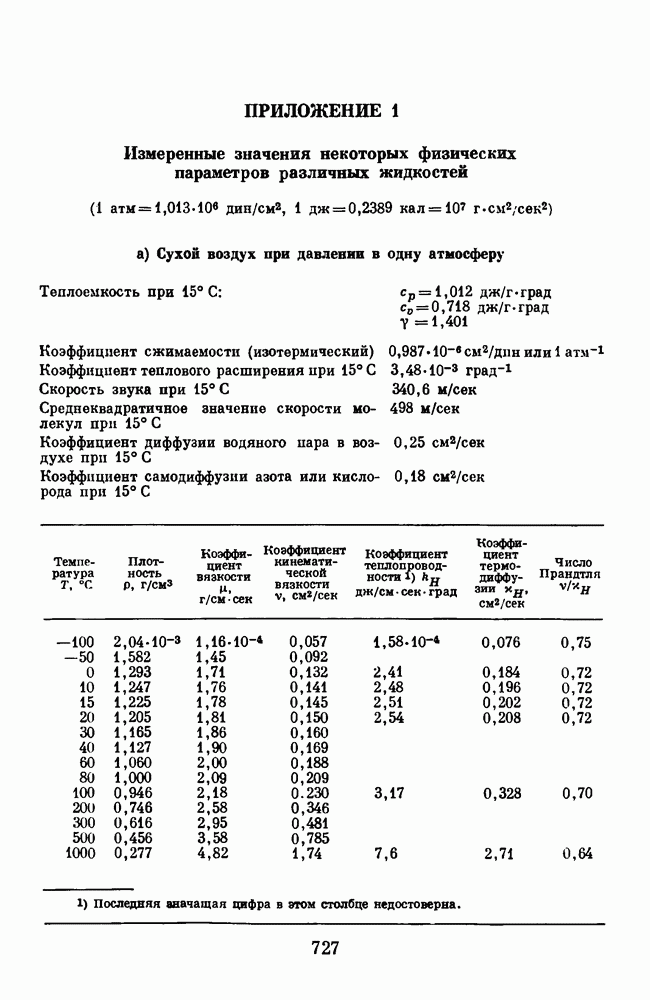
- ПРИЛОЖЕНИЕ 1. Измеренные значения некоторых физических параметров различных жидкостей
- ПРИЛОЖЕНИЕ 2. Выражения для некоторых векторных дифференциальных величин в ортогональных криволинейных координатах
- СПИСОК ЛИТЕРАТУРЫ